企业服务导航
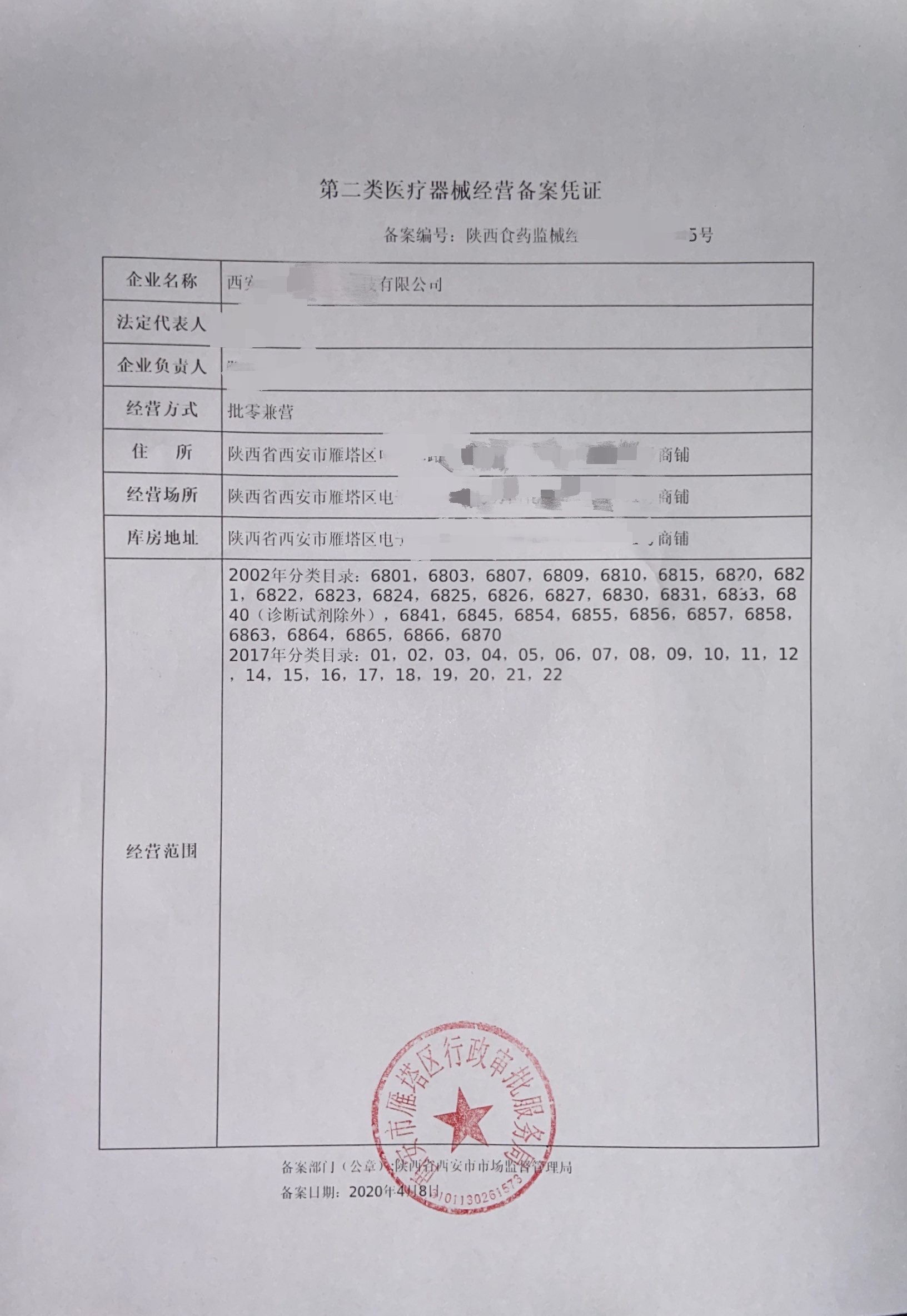
《医疗器械监督管理条例》(2000年1月4日国务院令第276号发布,2014年3月7日第680号修订,2017年5月4日予以修改)第三十条:从事第二类医疗器械经营的,由经营企业向所在地设区的市级人民政府食品药品监督管理部门备案并提交其符合本条例第二十九条规定条件的证明资料。《医疗器械经营监督管理办法》(国家食品药品监督管理总局令第8号)第八条; 第十二条 :从事第二类医疗器械经营的,经营企业应当向所在地设区的市级食品药品监督管理部门备案,填写第二类医疗器械经营备案表,并提交本办法第八条规定的资料(第八项除外)。 第十三条 :食品药品监督管理部门应当当场对企业提交资料的完整性进行核对,符合规定的予以备案,发给第二类医疗器械经营备案凭证。 第十四条 :设区的市级食品药品监督管理部门应当在医疗器械经营企业备案之日起3个月内,按照医疗器械经营质量管理规范的要求对第二类医疗器械经营企业开展现场核查。
办理时间
5个工作日
所需材料
1、营业执照副本
2、法定代表人、企业负责人、质量负责人的身份证明、学历或者职称证明复印件
3、经营场所平面图、房屋产权证明文件或者租赁协议(附房屋产权证明文件)复印件
4、其他证明材料
服务流程
签订合同---收集资料---完善材料---提交申请---审核通过---领证


![[field:title /]](/style/images/star.png)





